L’IA et la lutte contre le cancer : pourquoi il est difficile de l’utiliser pour le diagnostic
Examiner le corps humain pour détecter et diagnostiquer le cancer consiste à repérer des modèles. Les radiologues utilisent les rayons X et l’IRM pour éclairer les tumeurs, tandis que les pathologistes examinent les tissus des reins, du foie et d’autres zones au microscope à la recherche de modèles montrant la gravité de la tumeur, l’efficacité de traitements particuliers et la propagation possible de la maladie. néoplasme.
L’intelligence artificielle devrait pouvoir nous aider à faire ce travail. « Notre travail consiste à reconnaître des formes », dit-il Andrew Norgan, pathologiste et directeur médical de la plateforme numérique de pathologie de la Mayo Clinic. « Nous examinons la diapositive et collectons les informations qui se sont révélées importantes. »
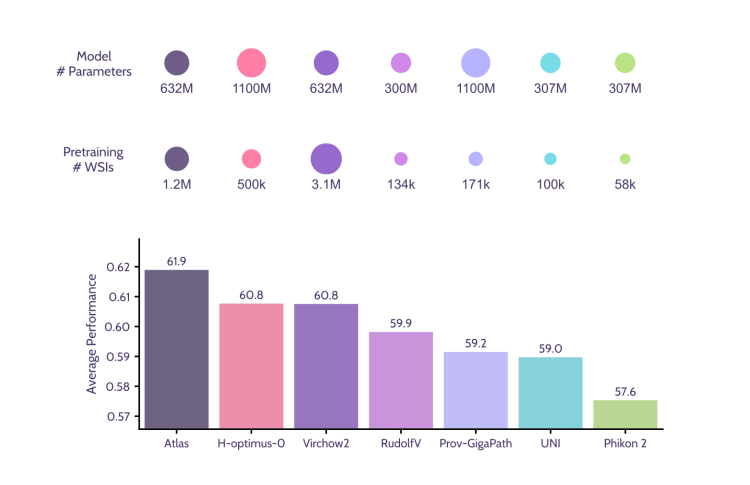
Aignostique et Mayo Clinic ont développé un modèle, appelé Atlas, Que il a battu les modèles concurrents dans six tests sur neuf.
L’IA fonctionne bien dans l’analyse visuelle
L’analyse visuelle est un domaine dans lequel l’IA est devenue très performante depuis que les premiers modèles de reconnaissance d’images ont commencé à décoller il y a près de 15 ans. Même si aucun modèle ne sera jamais parfait, on peut imaginer qu’un jour un algorithme puissant sera capable de détecter quelque chose qu’un pathologiste humain oublie, ou du moins d’accélérer le processus de diagnostic. Nous commençons à voir de nombreux nouveaux efforts pour construire un tel modèle – au moins sept tentatives au cours de la seule année dernière – mais ils restent tous expérimentaux. Que faudra-t-il pour les rendre suffisamment performants pour être utilisés dans le monde réel ?
Le modèle Atlas, voici ce qu’il peut faire
Au début de l’année 2025, ils étaient publié sur arXiv les détails de la dernière tentative de construction d’un tel modèle, menée par la société de soins de santé à intelligence artificielle Aignostique et la clinique Mayo. Le document n’a pas été évalué par des pairs, mais il en révèle beaucoup sur les défis liés à l’introduction d’un tel outil dans des contextes cliniques réels.
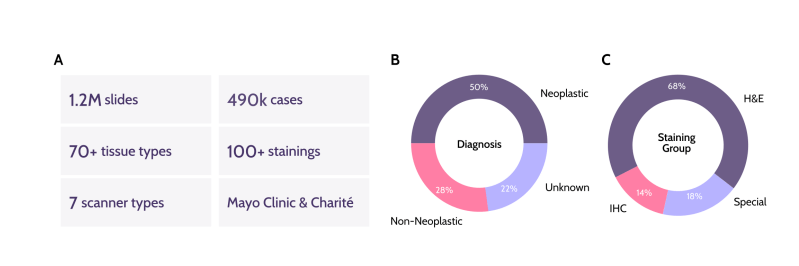
Le modèle, appelé Atlas, il a été formé sur 1,2 million d’échantillons de tissus provenant de 490 000 cas. Sa précision a été testée par rapport à six autres modèles pathologiques d’IA de pointe. Ces modèles s’affrontent sur des tests partagés, tels que la classification d’images de cancer du sein ou la classification de tumeurs, où les prédictions du modèle sont comparées aux réponses correctes fournies par des pathologistes humains. Atlas a obtenu le score le plus élevé dans la classification des tissus cancéreux colorectaux, arrivant à la même conclusion que les pathologistes humains dans 97,1 % des cas.
Cependant, pour une autre tâche, la classification des tumeurs issues de biopsies du cancer de la prostate, Atlas a battu les scores les plus élevés des autres modèles avec un score de seulement 70,5 %. Sa moyenne sur neuf tests de référence a montré qu’il obtenait les mêmes réponses que les experts humains dans 84,6 % du temps.
Réfléchissons à la signification de ces données. La meilleure façon de savoir ce qui arrive aux cellules cancéreuses dans les tissus est de demander à un pathologiste d’examiner un échantillon, c’est donc par rapport à ces performances que les modèles d’IA sont mesurés. Les meilleurs modèles se rapprochent des humains dans certaines tâches de détection, mais sont à la traîne dans de nombreuses autres.

Quelle doit être la qualité d’un modèle pour être cliniquement utile ?
« 90 %, ce n’est probablement pas suffisant. Nous devons être encore meilleurs », dit-il Carlo Bifulcomédecin-chef de Providence Genomics et co-créateur de GigaPathl’un des autres modèles de pathologie de l’IA examinés dans l’étude de la Mayo Clinic. Cependant, selon Bifulco, les modèles d’IA qui n’obtiennent pas de résultats parfaits peuvent quand même être utiles à court terme et pourraient potentiellement aider les pathologistes à accélérer leur travail et à poser des diagnostics plus rapidement.
Quels sont les obstacles qui vous empêchent d’améliorer vos performances ? Le problème numéro un est représenté par données de formation.
« Moins de 10 % des cabinets de pathologie aux États-Unis sont numérisés », explique Norgan. Cela signifie que les échantillons de tissus sont placés sur des lames et analysés au microscope, puis stockés dans d’énormes dossiers sans jamais être documentés numériquement. Même si les pratiques européennes tendent à se digitaliser et se poursuivent efforts Pour créer des ensembles de données partagés d’échantillons de tissus sur lesquels entraîner des modèles d’IA, il n’y a pas encore grand-chose sur lequel travailler.

Sans ensembles de données diversifiés, les modèles d’IA ont du mal à identifier le large éventail d’anomalies que les pathologistes humains ont appris à interpréter. Cela vaut également pour les maladies rares, explique-t-il Maximilien Alberco-fondateur et CTO d’Aignostics. En recherchant dans les bases de données publiques des échantillons de tissus provenant de maladies particulièrement rares, « vous trouvez 20 échantillons en 10 ans », explique Alber.
Le travail effectué par la Clinique Mayo
Vers 2022, la Mayo Clinic prévoyait que ce manque de données d’entraînement serait un problème. Elle a décidé de numériser tous ses dossiers pathologiques, ainsi que 12 millions de lames provenant de ses archives datant de plusieurs décennies (les patients avaient consenti à leur utilisation à des fins de recherche). Il a embauché une entreprise pour construire un robot qui commencerait à prendre des photos haute résolution de tissus, traitant jusqu’à un million d’échantillons par mois. Grâce à ces efforts, l’équipe a pu collecter 1,2 million d’échantillons de haute qualité utilisés pour entraîner le modèle de Mayo.
Cela nous amène au problème numéro deux : utiliser l’IA pour détecter le cancer. Les échantillons de tissus issus de biopsies sont minuscules, souvent de quelques millimètres de diamètre, mais ils sont tellement agrandis que les images numériques contiennent plus de 14 milliards de pixels. Cela les rend environ 287 000 fois plus grandes que les images utilisées pour former les meilleurs modèles de reconnaissance d’images IA.
« Cela signifie évidemment beaucoup de coûts de stockage, etc. », explique Hoifung Poon, chercheur en IA chez Microsoft qui a travaillé avec Bifulco pour créer GigaPath, publié dans Nature en 2024. Mais cela oblige également à prendre des décisions importantes quant aux parties de l’image à utiliser pour entraîner le modèle d’IA et aux cellules qui pourraient s’échapper au cours du processus.

Comment la clinique Mayo a construit Atlas
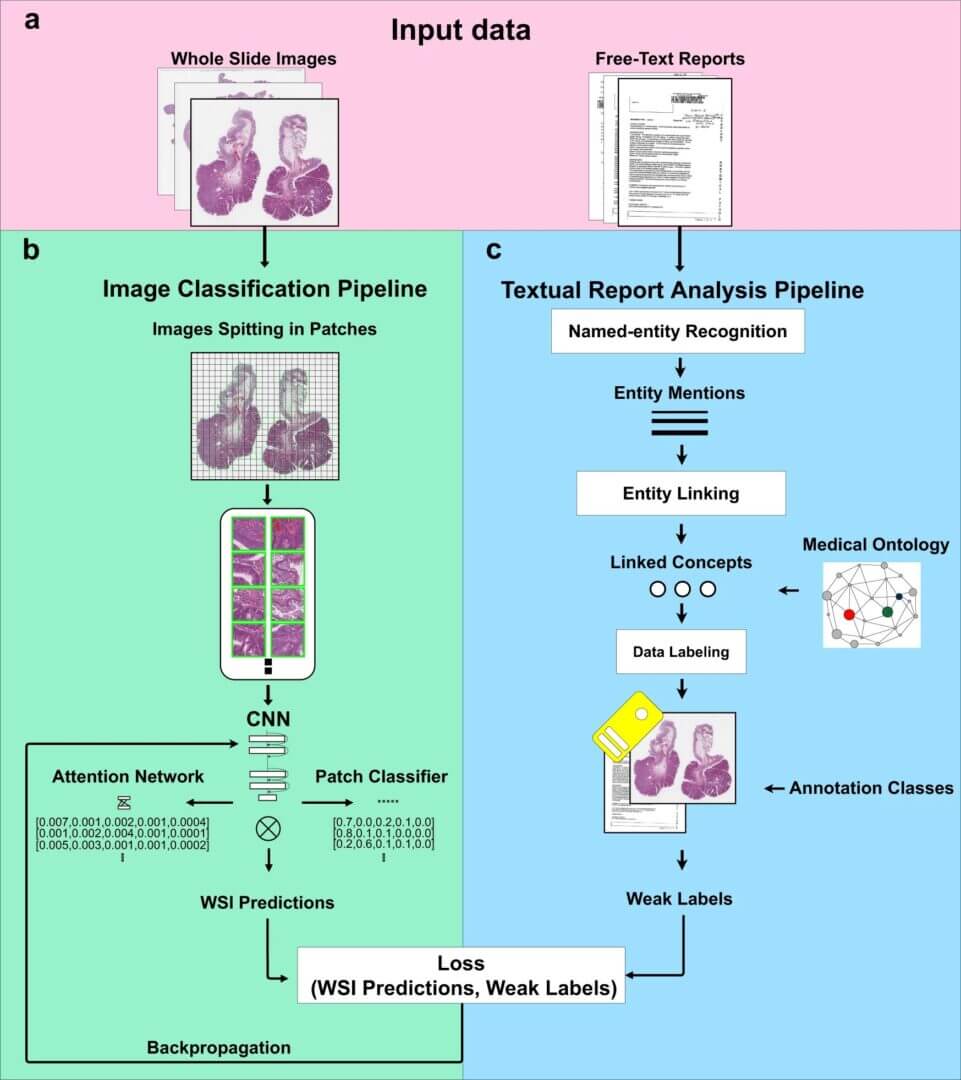
Pour fabriquer Atlas, la clinique Mayo a utilisé ce qu’on appelle méthode de tuilecréant essentiellement de nombreux instantanés à partir du même échantillon pour alimenter le modèle d’IA. Déterminer comment sélectionner ces carreaux est un art et une science, et on ne sait pas encore quelles sont les meilleures façons de le faire.
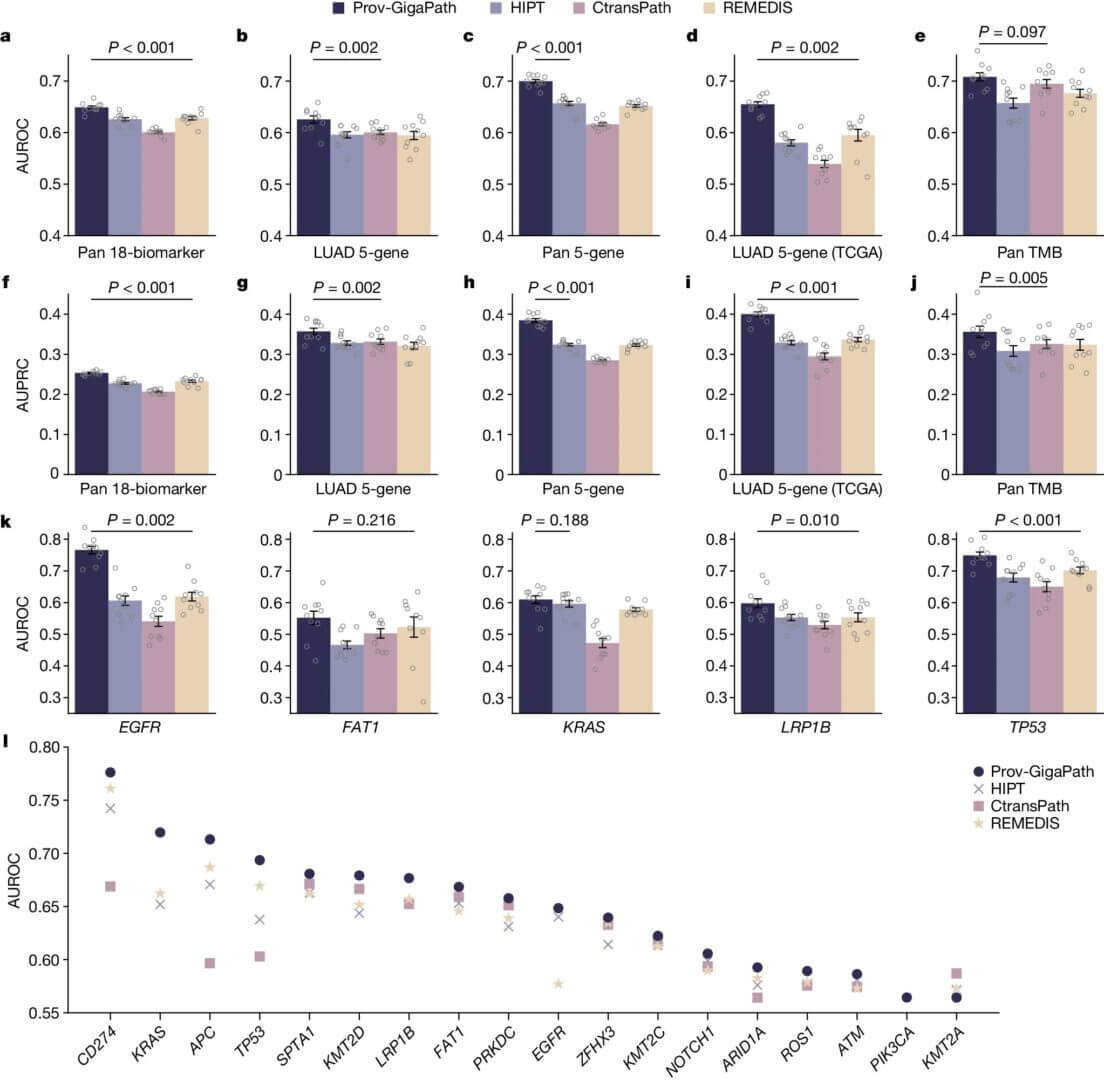
Troisièmement, se pose la question de savoir quels sont les critères les plus importants pour un modèle d’IA qui détecte le cancer. Les chercheurs de l’Atlas ont testé leur modèle dans le domaine difficile des références moléculaires, qui consiste à rechercher des indices à partir d’images d’échantillons de tissus pour deviner ce qui se passe au niveau moléculaire.
Voici un exemple : les gènes de réparation des mésappariements du corps sont particulièrement inquiétants pour le cancer, car ils détectent les erreurs commises lors de la réplication de l’ADN. Si ces erreurs passent inaperçues, elles peuvent favoriser le développement et la progression du cancer.
« Certains pathologistes pourraient dire qu’ils ont une sorte de sentiment lorsqu’ils pensent que quelque chose manque de réparation en fonction de son apparence », explique Norgan. Mais les pathologistes n’agissent pas uniquement sur ce sentiment. Ils peuvent effectuer des tests moléculaires pour obtenir une réponse plus définitive. Et si, dit Norgan, nous pouvions utiliser l’intelligence artificielle pour prédire ce qui se passe au niveau moléculaire ? C’est une expérience : le modèle d’IA pourrait-il détecter des changements moléculaires sous-jacents que les humains ne peuvent pas voir ?
Généralement non, semble-t-il. Ou du moins pas encore. La moyenne d’Atlas pour les tests moléculaires était de 44,9 %. Il s’agit du meilleur résultat obtenu jusqu’à présent par l’intelligence artificielle, mais cela montre que ce type de tests a encore un long chemin à parcourir.
Selon Bifulco, Atlas représente un progrès progressif mais réel. « Mon sentiment, malheureusement, c’est que tout le monde est coincé au même niveau », dit-il. « Nous avons besoin de quelque chose de différent en termes de modèles pour réaliser des progrès réellement significatifs, et nous en avons besoin d’ensembles de données plus volumineux».

